Pfizer, chiesto ok Usa a vaccino Omicron 4-5, in Ue nei prossimi giorni
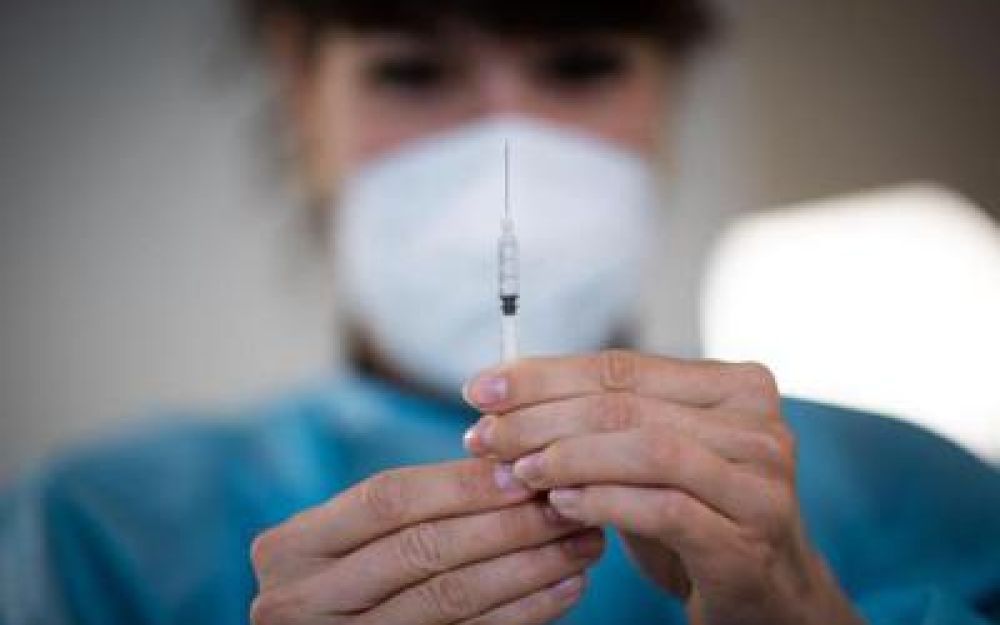
Milano, 22 ago. (Adnkronos Salute) – Pfizer e BioNTech hanno presentato negli Usa, alla Fda, la richiesta di autorizzazione all’uso di emergenza del vaccino anti-Covid bivalente adattato per Omicron 4/5. A darne notizia sono le due aziende in una nota. “Pianifichiamo di completare la presentazione all’Agenzia europea del farmaco Ema” della richiesta di autorizzazione condizionata all’immissione in commercio “nei prossimi giorni”, aggiunge via Twitter il presidente e Ceo di Pfizer. La domanda presentata negli Usa richiede il via libera al vaccino aggiornato per l’utilizzo di una dose di richiamo di 30 microgrammi in persone di età dai 12 anni in su.
La domanda presentata negli Usa include i dati clinici del vaccino bivalente adattato per Omicron BA.1 e i dati preclinici e di produzione del vaccino bivalente adattato a Omicron BA.4/BA.5. “L’agilità della piattaforma mRna”, commenta Bourla, “ci ha permesso di sviluppare, testare e produrre vaccini aggiornati che si allineano ai ceppi circolanti con una velocità senza precedenti. Avendo aumentato rapidamente la produzione, siamo posizionati per iniziare immediatamente la distribuzione dei booster bivalenti Omicron BA.4/BA.5, se autorizzati”.
E’ “di grande importanza che i vaccini possano essere adattati rapidamente ai principali lignaggi di Omicron circolanti”, aggiunge Ugur Sahin, Ceo e co-fondatore di BioNTech. “In meno di tre mesi dopo che la Fda ha fornito la sua guida per i vaccini adattati negli Stati Uniti, siamo pronti a spedire le prime dosi del nostro vaccino bivalente Omicron BA.4/BA.5, in attesa dell’autorizzazione regolatoria”. Il vaccino bivalente contiene mRna che codifica per la proteina spike originale di Sars-CoV-2, presente nel vaccino originario di Pfizer-BioNTech, insieme all’mRna che codifica per la proteina spike della variante Omicron 4 e 5.
I dati preclinici, si legge nella nota diffusa dalle aziende, “hanno mostrato che una dose booster del vaccino bivalente adattato a Omicron BA.4/BA.5 genera una forte risposta anticorpale neutralizzante contro le varianti Omicron BA.1, BA.2 e BA.4/BA.5, così come per il ceppo originario. Uno studio clinico che esaminerà la sicurezza, la tollerabilità e l’immunogenicità del vaccino bivalente Omicron BA.4/BA.5 in over 12 dovrebbe partire questo mese.
La Ragione è anche su WhatsApp. Entra nel nostro canale per non perderti nulla!
Leggi anche


Dengue e malaria, boom di casi: è colpa del clima, allarme infettivologi


Disturbi della memoria, scoperto come il cervello distingue e conserva eventi simili


Torracca (Apacs): “Formare pazienti e medici per diagnosi precoce Egpa”